Véritable géant des rivières, le Silure de chez nous, de son vrai nom Silurus glanis alias le silure glane, faait débats au sein des communautés de pêcheurs mais également en dehors de la sphère de la pêche de loisir. Il est aussi bien détesté qu’apprécié : certain le considère « nuisible », d’autre prône sa place au sein de l’écosystème. Mais alors, qui est le Silure ? On y répond sur la base des études scientifiques spécifiques à son sujet.
Pour commencer: une espèce native ou introduite ?
Des travaux en archéologie en Alsace et en Belgique, couplés à l’examen de la littérature ancienne, ont mis en évidence la présence naturelle du silure dans les bassins du Rhin, de la Meuse et de l’Escaut, durant l’âge de bronze (vers 2459 – 2206 av. J.-C.) et l’Antiquité . En l’occurrence, le silure glane était naturellement présent dans ces bassins versants après les dernières glaciations (- 9000 ans) et doit être considéré comme « natif » sur ces bassins.
Sur le bassin du Rhône, les chercheurs ont mis en évidence la présence de fossiles datant du Miocène mais qui ne peut justifier du caractère « natif » de l’espèce dans ce territoire dans la mesure où il s’agit d’autres espèces de silure, désormais éteintes.
Pourtant cette espèce est aujourd’hui établie dans de nombreux cours d’eau et plans d’eau de plaine en France, car il a fait l’objet de (ré)introductions.

Historique des introductions :
Alors que le silure, à l’état « natif » dans les bassins du Rhin à l’Escaut, a disparu à la fin du Moyen-Âge, des tentatives de réintroductions ont été menées dès la fin du XVIIIe siècle en Alsace, sans succès. La première tentative d’introduction documentée en France date de 1857 via la pisciculture de Huningue en Alsace. Il est ensuite largement introduit dans le bassin du Doubs vers 1890 et dans le canal du Rhône au Rhin, sans pour autant que les populations se maintiennent.
De nouvelles introductions à des fins aquacoles ont eu lieu en 1956 dans le bassin de la Saône, puis en Camargue en 1981-82, aboutissant à la colonisation du bassin du Rhône. Ainsi, les premières introductions du silure en France auront été principalement motivées par un intérêt aquacole et par la « curiosité zoologique », encouragée par la société nationale d’acclimatation pour l’introduction de nouvelles espèces à la fin du XIXe siècle.
Il s’en suit alors une dissémination dans de nombreux cours d’eau et plan d’eau, avec une explosion démographique à partir de la fin des années 1990.
Aujourd’hui, le statut du silure glane est « natif (indigène) », car en se positionnant à l’échelle de la France, l’espèce est démontrée comme étant native sur au moins un territoire local.
Sa dynamique de population
L’évolution des effectifs de silure a été particulièrement étudiée sur le bassin de la Garonne sur la période 1995 – 2017. Le silure a connu une phase d’expansion très marquée entre les années 2000 et 2012, phase qui semble s’être interrompue, avec une aire de distribution et des effectifs stables depuis quelques années dans ce bassin.
Cependant, dans le cas des passes à poisson de type « bassins », les chercheurs ont mis en évidence une tendance à la hausse des effectifs annuels de silure. Néanmoins, il existe des biais à cette étude notamment le fait que les périodes étudiées ne sont pas les mêmes et que certains individus séjournent plusieurs jours dans les passes à poissons en faisant plusieurs allers-retours devant le système de vidéo-comptage et donc comptés plusieurs fois.
Un rôle de top prédateur
Son régime alimentaire :
Les nombreuses études sur le régime alimentaire au stade adulte font état d’un régime à dominante piscivore mais aussi opportuniste : le silure tend à se nourrir des espèces les plus abondantes ou les plus accessibles (présentant les meilleures chances de capture).
Mais les contenus stomacaux présentent ainsi une grande diversité taxonomique : outre du poisson, on y trouve aussi des crustacés (p. ex. écrevisses), des amphibiens, des oiseaux (p. ex. cormoran), des mollusques (p. ex. corbicules), des mammifères, des déchets organiques etc.
Mais il existe une forte variabilité entre les sites et entre les années. La part des poissons apparaît plus importante dans le régime alimentaire des silures de la Dordogne que ceux de la Garonne, de la Dordogne aval et de la Loire, lesquels consommeraient relativement plus d’invertébrés (Figure 2A). Les invertébrés consommés sont notamment composés d’écrevisses exotiques (Procambarus clarkii ou Faxonius limosus) et de corbicules (Corbicula spp).
Enfin, Faure & Tanzilli (2016) ont observé que les gros spécimens de silure (> 170 cm) pouvaient s’attaquer aux plus petits mais ce cannibalisme apparait non systématique et dans des proportions variables d’un bassin à un autre.
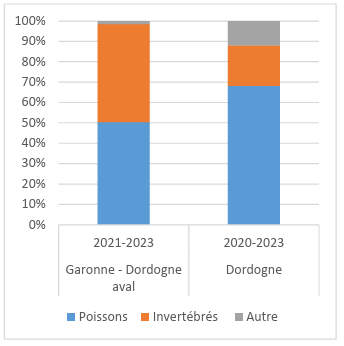
Composition des types de proies consommées par Silurus glanis
En période de migration des poissons amphihalin (alose, anguille, lamproies marines), ces espèces font donc partie de son régime alimentaire. A ces périodes de migrations, les espèces de poissons migrateurs représenteraient alors :
- 53-65% du régime sur la Garonne
- 30-55% du régime sur la Loire (chez des individus de silure > 1.2m)
- 8% de proies marines sur la Vilaine.
Mais là encore, la contribution des migrateurs amphihalins dans le régime alimentaire des silures varie entre 10 et 95% selon les individus et la saison.
La consommation de géniteurs d’amphihalins semble également dépendre de la taille des silures : ceux de plus de 120 cm étant plus susceptibles d’en consommer.
En Camargue spécifiquement, plusieurs études ont essayé de mettre en relation la chute des densités d’anguilles avec l’augmentation des densités de silure observée. Mais cet effet direct n’a pas pu être expliquée par la prédation, car une étude montre une consommation anecdotique de proies marines (=anguilles). Ces résultats renforcent l’idée que le silure ne cible pas nécessairement les amphihalins mais les espèces les plus accessibles.
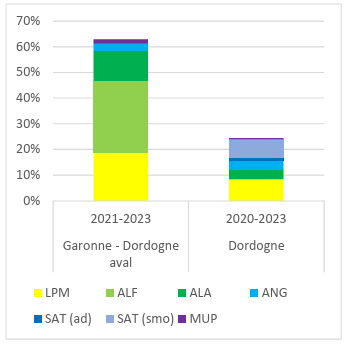
Part des poissons migrateurs dans la consommation de "poissons" des silures
Compétition entre les prédateurs ?
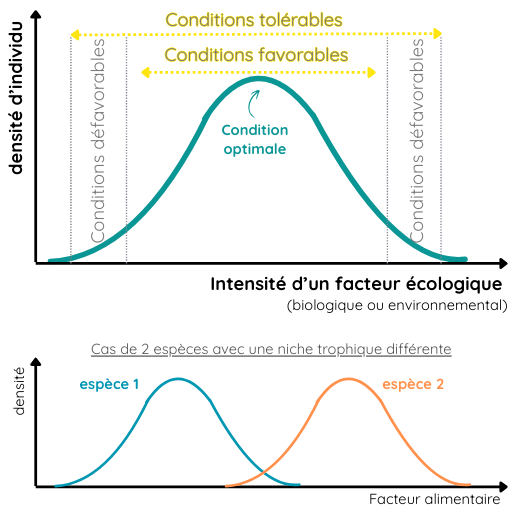
Schémas théoriques pour illustrer la notion de « niche écologique »
Avec la présence de brochets, de sandres ou encore de perches dans nos milieux, qui sont également des espèces prédatrices, on pourrait se questionner s’il n’y a pas une compétition pour la ressource alimentaire entre les silures et les autres espèces.
Certains suggèrent une compétition entre les jeunes silures et le brochet, ou encore que le silure et l’anguille consomment souvent les même proies (cas de l’écrevisses de Louisianne en Camargue), alors que d’autres études montrent que les différents juvéniles de sandre, silure, perche et brochet arrivent à se répartir leur niche trophique.
Une niche trophique est la diversité des ressources alimentaires exploitées et nécessaires à une espèce, qui est une des nombreuses composantes de sa niche écologique. Ainsi, 2 espèces entrent en compétition quand elles ont une partie de leur niche écologique qui se supperpose.
Au final, il semblerait que les impacts de cette compétition restent limités, probablement grâce une niche trophique plus large et plus flexible chez le silure.